行业动态丨国家药监局药品审评中心CDE6月受理9项细胞治疗新药!中国细胞治疗迎来关键加速期!
点击蓝字 关注我们

前 言
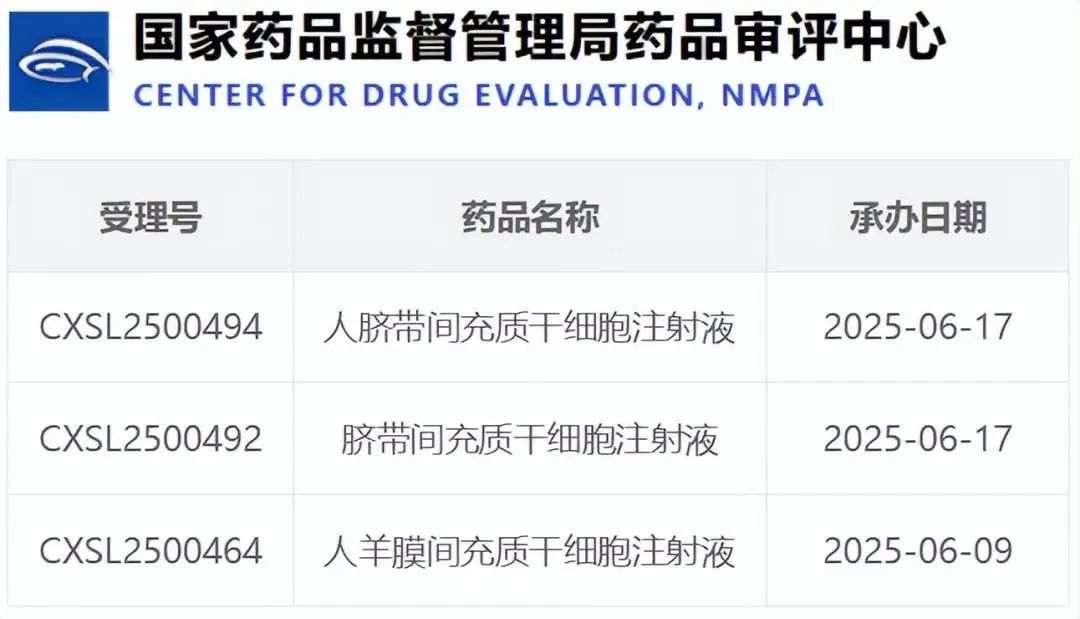
2025年6月,中国细胞治疗发展迎来一个重要信号:国家药品监督管理局药品审评中心(CDE)共受理9项细胞治疗新药临床试验申请,涵盖间充质干细胞(MSC)、CAR-T、CAR-NK、树突状细胞(DC)等多条核心技术路径。
这不是一次简单的数据堆积,而是中国细胞治疗由“散点式突破”转向“系统化布局”的标志性节点。监管提速、路径清晰、适应症扩展,预示着细胞治疗产业正进入一个多线并行、加速兑现的全新阶段。从修复组织、调节免疫到清除肿瘤,这些细胞药物正在拓宽医学的边界,也为众多难治性疾病带来前所未有的治疗可能。
01
干细胞产品稳步推进,瞄准疑难病与慢性炎症
本月获批的三款间充质干细胞(MSC)治疗产品,分别用于类风湿性关节炎、脑损伤和肝硬化等重大疾病,显示出干细胞在“组织再生+免疫调节”双重机制下的广泛应用潜力。
类风湿等自身免疫疾病,往往缺乏根治方案,而干细胞通过分泌抗炎因子、抑制免疫攻击、修复受损组织,有望从机制层面“打断”病程循环。脑损伤与肝纤维化等病变,亦存在传统治疗效果有限、恢复周期长的难题。研究显示,干细胞在动物模型中可促进神经再生、改善肝功能,是当前国际研究热度最高的靶点领域之一。

这类产品的临床布局,意味着中国干细胞治疗已不再局限于美容、骨关节等传统领域,而是正在向更复杂、治疗难度更高的系统性疾病深入拓展。从疗效预期、制造标准到风险控制,干细胞产品已经形成较为成熟的监管路径,是当前细胞治疗领域最具普适性的基础力量。
02
CAR-T疗法继续深耕,精细化分型成主流方向
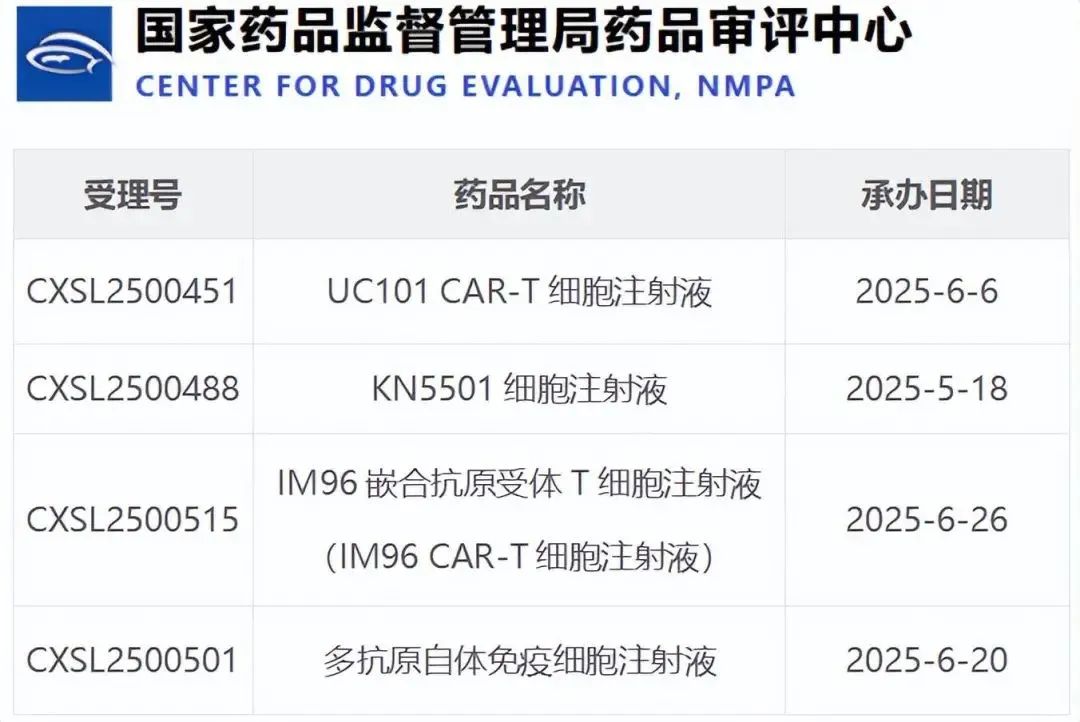
在9项受理的新药中,4项属于CAR-T疗法,显示其在细胞治疗中的核心地位仍旧牢固。与过去追求“广谱抗癌”的思路不同,如今的CAR-T产品更多聚焦于特定癌种与靶点,靶向B细胞恶性肿瘤、血液系统疾病甚至某些实体瘤。通过优化识别元件、降低副作用、提升持续性,CAR-T正走向“个体精准+平台化开发”的阶段。
值得注意的是,这批CAR-T产品均针对不同靶点、不同适应症,呈现出“靶点清晰+机制稳定+路径清楚”的研发格局。这种以靶点为导向的研发策略,既符合CDE当前审评趋势,也更有利于临床试验数据的积累和评估,缩短从实验室到医院的转化周期。
数据显示,截至2024年底,中国CAR-T临床项目已突破200项,部分已进入II/III期试验,显示出整个赛道正逐步由“创新引爆期”走向“验证落地期”。
03
CAR-NK与DC疫苗首次集体登场,
免疫治疗进入“组合作战”阶段
6月的细胞治疗受理名单中,首次出现CAR-NK和DC疫苗类新药,标志着中国免疫细胞治疗不再只是“T细胞独角戏”,而是正式进入“多细胞联合作战”的新格局。
CAR-NK是一种将抗癌基因工程引入自然杀伤细胞的疗法,具有“无需配型、毒性更低、成本可控”的先天优势,在国际上被视为CAR-T之外的有力补充。
而DC疫苗(树突状细胞疫苗)则通过激活患者体内的T细胞群体,提升其识别和清除肿瘤的能力,适用于需要“主动激活免疫反应”的实体瘤治疗。
这类新技术的受理,说明中国监管机构正在接纳更丰富的免疫干预机制,建立多元产品评价体系。
这不仅拓宽了治疗工具箱,也对研发企业提出更高标准——谁能率先实现“机制清楚、标准统一、可规模放大”,谁就能在新一轮免疫疗法竞赛中脱颖而出。
更重要的是,CAR-NK、DC疫苗等疗法更适合与其他治疗方式联用,为未来组合疗法(combo therapy)铺平道路,开启“多维免疫干预”的新纪元。
04
监管体系全面提速,细胞新药审评步入“高效期”
相较于以往的长周期、不确定性审批路径,6月细胞新药集中受理背后,是中国药审体系在制度层面持续优化的成果。一方面,CDE已构建起覆盖细胞制备、质量控制、风险评估、适应症匹配的完整评审框架;另一方面,细胞治疗作为国家鼓励类前沿技术,正享受包括绿色通道、滚动评审、条件性上市等多项制度红利。
尤其值得关注的是,此次获受理的9款新药分属不同技术路线,但审评节奏基本同步完成,体现了监管部门已具备“路径识别+并行评估”的实战能力。这对于企业而言,意味着不再受制于审批瓶颈,创新产品可以更快进入临床、验证疗效、服务患者。而对于临床医生和患者来说,则带来更加多样的治疗选择,打破“无药可用”“用药滞后”的传统瓶颈。
2023年底,中国药审中心正式发布《细胞治疗产品审评技术指导原则(试行)》,提出“循证路径+数据主导”的新模式,为后续审评标准化、效率化奠定基础。本轮IND密集受理,正是这一新机制落地实施的结果,也是产业规范化、技术产品化的真实信号。
05
不是风口,是通道——细胞治疗进入战略兑现期
细胞治疗从概念提出至今,经历了起步、爆发、冷静,再到今天的集中提速。MSC、CAR-T、CAR-NK、DC疫苗,不再是“明星新词”,而是一个个正在走进临床、走进医院、走进患者的现实药物。
从技术储备到审评通道,从产业共识到政策利好,中国的细胞治疗正步入战略兑现的关键时期。监管机构的高效作为,标志着一个“创新驱动+制度护航”的时代已经来临。这一次,它不是风口,而是一条通道;不是设想,而是兑现;不是未来,而是现在。

本篇文章来源于微信公众号:中启源生物科技







