细胞科普丨Cell子刊:5年生存率仅6%的神经胶质瘤,NK细胞疗法从多个维度取得突破
点击蓝字 关注我们

引言
在人类与癌症的漫长斗争中,有一种肿瘤如同“终极噩梦”般存在——神经胶质瘤(Glioblastoma, GBM),尤其是儿童高发的弥漫性内生性脑桥胶质瘤(DIPG),更是被冠以“癌中之王”的恶名。
这种肿瘤的可怕之处并非在于其生长速度,而在于其难以攻克的特性,仿佛是“打不死的小强”。尽管放疗、化疗、靶向药物等常规治疗手段都已尝试,但患者的生存期却始终难以突破12至18个月的瓶颈。
然而,2025年发表在《Molecular Therapy》(Cell子刊)上的一篇综述文章,为我们带来了全新的希望,提出了一种“多维战术”——利用NK细胞从多个维度围剿这一不死顽敌。
文章指出,自然杀伤细胞(NK细胞)不仅能够精准识别并杀伤神经胶质瘤干细胞,还借助CAR技术、细胞接合器、外泌体等多种方式,成功跨越血脑屏障,清除肿瘤微环境中的免疫抑制因素,正在成为攻克“最难治癌症”的全新突破口。
这并非仅仅是“又一种免疫疗法”,而是免疫疗法领域的一次革命性突破。
01
为什么神经胶质瘤难治?
它不是普通肿瘤,是有“干细胞指挥部”的战争堡垒
如果说肺癌、乳腺癌是“局部战斗”,那么神经胶质瘤则是一场“持久战+游击战”。真正让神经胶质瘤难以治愈的,不是肿瘤本身,而是隐藏在肿瘤深处的一小撮“元凶”——胶质瘤干细胞(Glioma Stem-like Cells, GSCs)。
这些细胞具有三大显著特点:
高度异质性与伪装性:它们能够分化成各种不同类型的肿瘤细胞,抗原表达极不稳定,这使得它们能够轻易逃逸传统免疫系统的识别,仿佛是肿瘤中的“伪装者”。
对放疗、化疗“天然免疫”:它们拥有极强的DNA修复能力和耐药性,这使得常规的放疗和化疗难以对其产生有效杀伤,正是这些细胞导致了肿瘤的反复复发和治疗的最终失败。
强侵袭性和微环境操控力:GSCs能够重编程肿瘤微环境,诱导血管新生,并释放免疫抑制因子(如TGF-β、IL-10),从而使T细胞失去作用,巨噬细胞“倒戈”,为肿瘤的生长和扩散提供了有利条件。
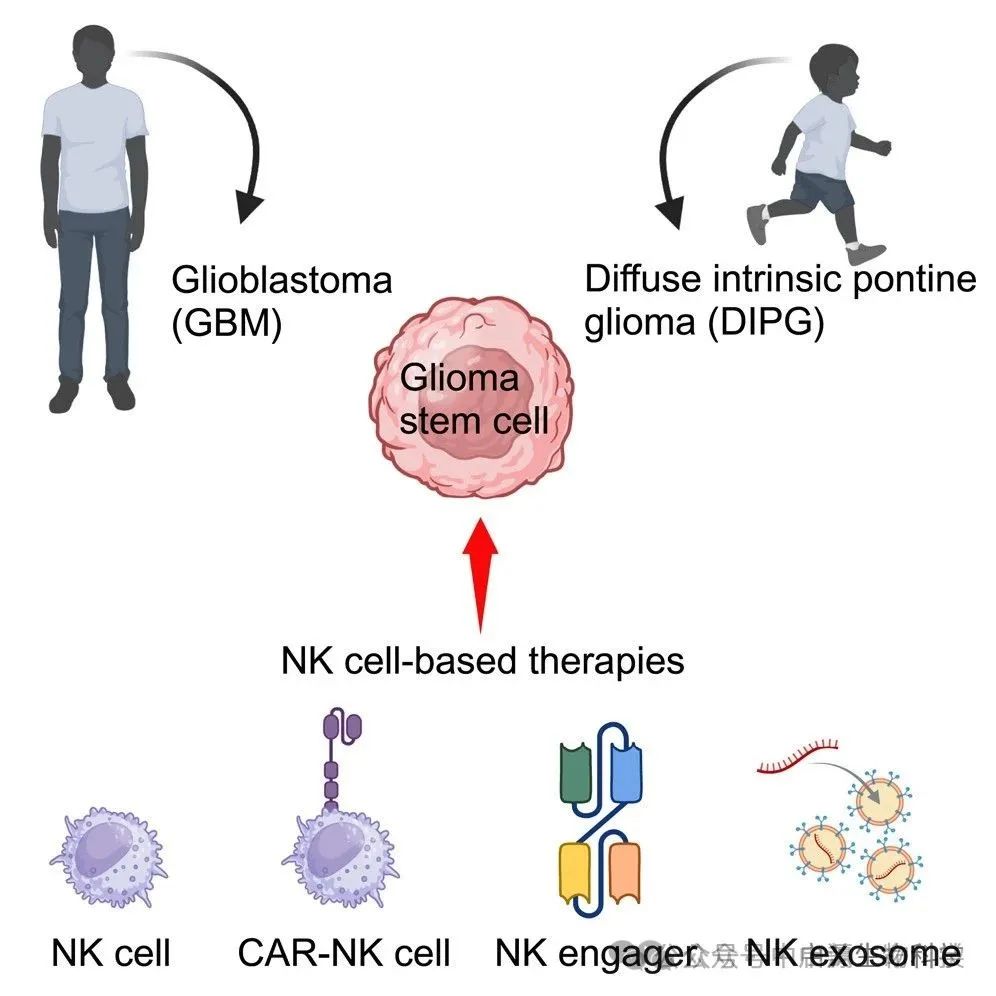
▲图解摘要
研究发现,即使外科手术清除了99%的肿瘤体积,只要有一小撮胶质瘤干细胞(GSC)残存,肿瘤就能迅速卷土重来。这也正是神经胶质瘤5年生存率低于6%,而弥漫性内生性脑桥胶质瘤(DIPG)几乎没有治愈记录的关键原因。
传统免疫疗法,如PD-1抗体、CAR-T细胞疗法等,在面对这些“深藏不露”的GSC时,常常显得无能为力。
然而,NK细胞却与众不同。它并不依赖抗原识别,而是通过感知“危险信号”来发挥作用。GSCs隐藏得越深,NK细胞反而越能敏锐地察觉到它们的存在。这为我们提供了一个全新的思路:以NK细胞为武器,精准锁定肿瘤干细胞,打破这种“治不死”的恶性循环,为神经胶质瘤的治疗带来新的希望。
02
CAR-NK细胞,如何变成“特种部队”
精准刺杀胶质瘤干细胞?
要攻克神经胶质瘤干细胞(GSCs)这一“暗藏的指挥部”,仅依靠普通NK细胞的“天然反应”是远远不够的。于是,科学家们开始对它们进行“武装改造”,打造出更精准、更持久的版本——CAR-NK细胞。
CAR,即嵌合抗原受体(Chimeric Antigen Receptor),最初是为T细胞设计的,如今被成功移植到NK细胞上。这种改造使得CAR-NK细胞成为一支具备强大功能的免疫特种部队:它们能够精准识别靶点,发动自杀式突击,并在完成任务后安全撤退。
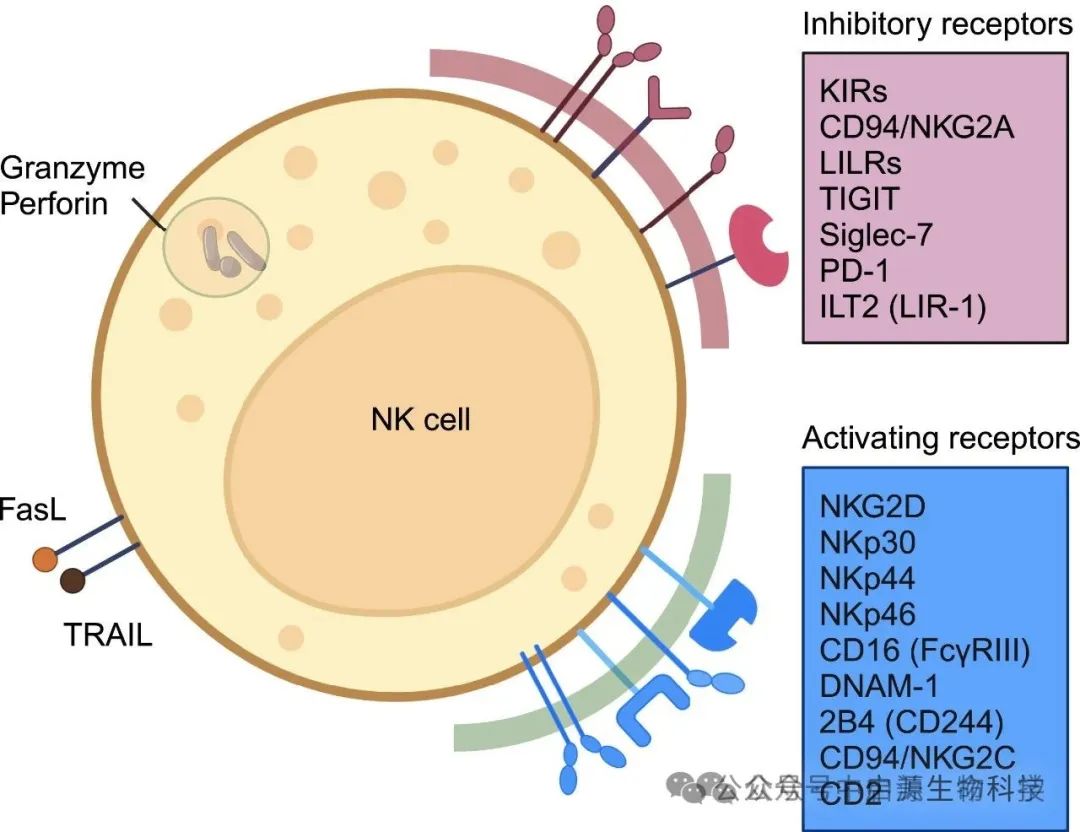
▲ NK细胞抑制和激活受体
2025年,《Molecular Therapy》杂志的综述文章详细介绍了CAR-NK细胞治疗神经胶质瘤的多项关键进展:
在靶点识别上,CAR-NK细胞能够精准锁定胶质瘤细胞表面的EGFRvIII、GD2、IL13Rα2等肿瘤特异性抗原,同时巧妙避开正常脑组织,实现精准打击。
在武器升级方面,通过携带IL-15基因,CAR-NK细胞获得了强大的“续航能力”,显著延长了其在体内的存活时间,增强了持续杀伤肿瘤细胞的能力。
在细胞来源上,CAR-NK细胞可以从脐带血、诱导多能干细胞(iPSC)中大量扩增,支持“现货型”临床应用,不再像CAR-T细胞那样依赖个体采集,大大提高了治疗的可及性和便捷性。
在安全性上,CAR-NK细胞几乎不引起细胞因子风暴(CRS)和神经毒性,特别适合用于“空间狭窄且脑组织脆弱”的中枢神经系统,显著降低了治疗风险。
在动物实验中,CAR-NK细胞在小鼠模型中展现出对胶质母细胞瘤(GBM)的完全缓解能力,并在弥漫性内生性脑桥胶质瘤(DIPG)的早期干预中显示出延缓肿瘤进展和减少神经损伤的巨大潜力。
简而言之,CAR-NK细胞比普通NK细胞更聪明,比CAR-T细胞更温和,是实体瘤免疫治疗中难得的“理智进攻型”疗法。而且,它并非停留在理论设想阶段,已有初步临床数据证实了其可行性。
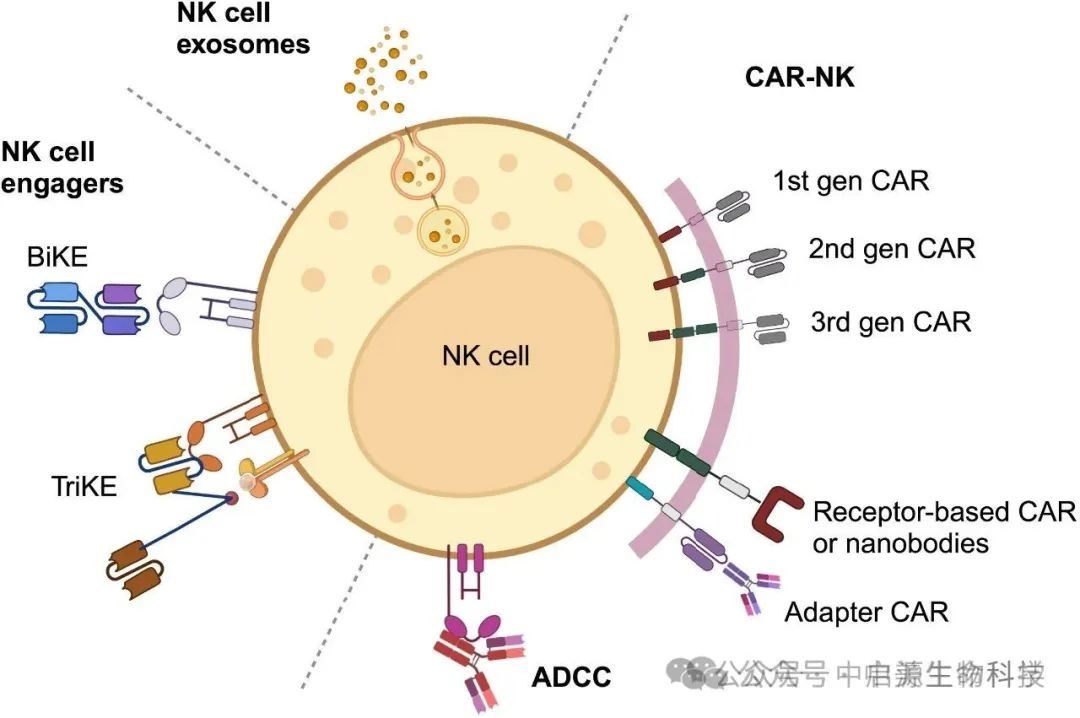
▲基于NK细胞的癌症疗法
03
NK细胞接合器,如何“一箭三雕”放大NK杀伤力?
除了“全副武装”的CAR-NK细胞,科学家们还开发出一种更加灵巧、更具模块化的新型工具——NK细胞接合器(NKCEs),也被称为biKEs(双特异性)和triKEs(三特异性)。
其原理犹如为NK细胞配备了一款“自动导航武器”:一端能够精准识别肿瘤抗原(例如EGFR、B7-H3、GD2),另一端则牢牢抓住NK细胞表面的激活受体(例如CD16、NKG2D)。对于triKE而言,中间还嵌入了IL-15分子,进一步增强NK细胞的增殖能力和持久性。
这种设计实现了“识别—激活—增殖”三位一体的闭环作战模式,极大地提升了NK细胞的抗肿瘤效果。
最新的研究亮点包括:
一款针对EGFRvIII/CD16的双特异性接合器在胶质母细胞瘤(GBM)小鼠模型中,成功使肿瘤体积缩小了72%,且未观察到明显的神经毒性副作用;
一款靶向B7-H3的triKE接合器正在用于弥漫性内生性脑桥胶质瘤(DIPG)的前临床实验。其独立激活NK细胞、穿越血脑屏障并在肿瘤区域富集的能力,受到了广泛关注;
与CAR-NK细胞相比,NKCEs不依赖细胞基因改造,能够实现批量生产,成本更低,临床推进速度也更快。
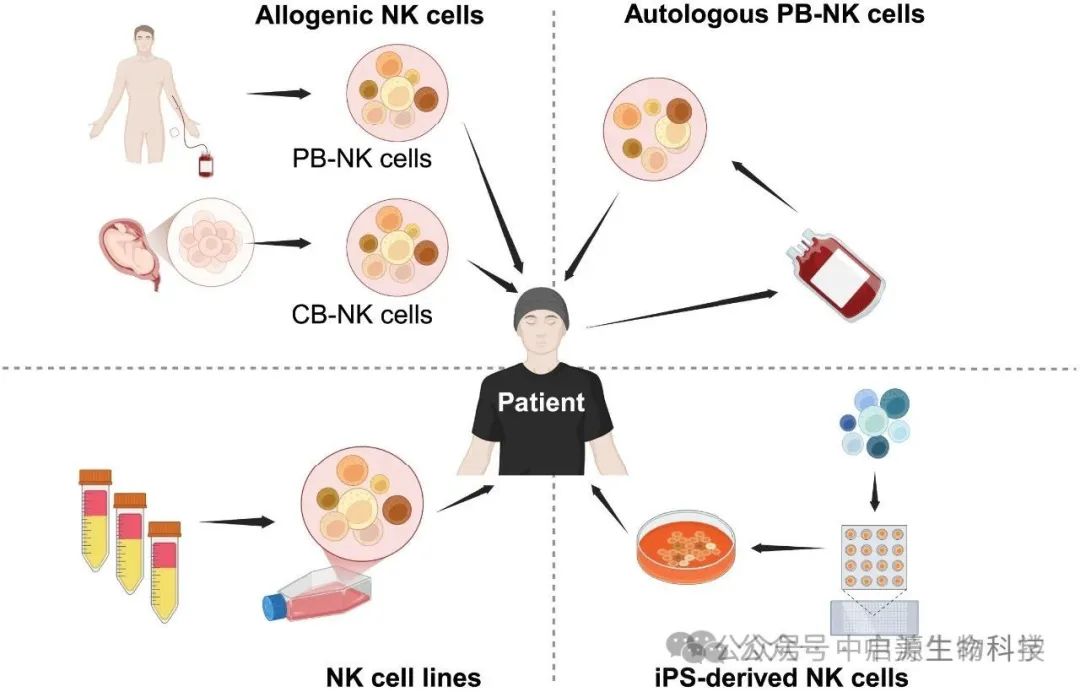
▲用于癌症免疫治疗的NK细胞来源
在医学领域,它被称为“合成生物学平台”;而在军事化的比喻中,它宛如一枚精准的“免疫激活导弹”。一旦锁定目标,它会瞬间释放杀伤信号,精准打击肿瘤细胞,几乎不存在误伤正常细胞的风险。
最关键的是,这种“外接武器”模式可以与CAR-NK细胞疗法叠加使用,形成“远程打击+近距离围剿”的强大组合疗法。这意味着,NK细胞不仅能被武装升级,还能通过这种外接方式实现“远程操控”,从而全方位突破胶质瘤干细胞的防线,为战胜这一顽疾带来新的希望。
04
NK细胞外泌体——穿透血脑屏障的“纳米突击队”
尽管CAR-NK细胞和NKCEs在抗肿瘤治疗中表现出色,但在面对神经胶质瘤的一大难题——血脑屏障(BBB)时,仍存在一定的物理限制。血脑屏障如同一道坚固的城墙,阻挡了大部分药物和细胞进入大脑组织,使得治疗效果大打折扣。
于是,科学家们将目光转向了一种更微型、更具穿透力的武器系统:NK细胞外泌体(NK-derived Exosomes)。
NK细胞外泌体是NK细胞自然分泌的微小囊泡,直径仅30-150纳米。别看它们个头小,但杀伤力毫不逊色,内部富含穿孔素、颗粒酶、IFN-γ等强大的免疫武器,能够精准引导肿瘤细胞凋亡。
更重要的是,NK细胞外泌体具有两大显著优势:
-
卓越的穿透能力:它们能够轻松穿越血脑屏障。《Molecular Therapy》杂志的综述文章指出,与CAR细胞和抗体分子相比,NK细胞外泌体更容易通过BBB,并在肿瘤区域高效富集,实现真正的“非侵入式递送”。
天然的安全性:NK细胞外泌体具有极低的毒性和免疫原性。它们不会引发炎症风暴,无需进行复杂的免疫配型,可以多次给药、反复使用,特别适合儿童脑瘤(如DIPG)等对安全性要求极高的治疗场景。
NK细胞外泌体的这些特性,使其成为突破血脑屏障、精准治疗神经胶质瘤的有力候选,为攻克这一难题带来了新的希望。
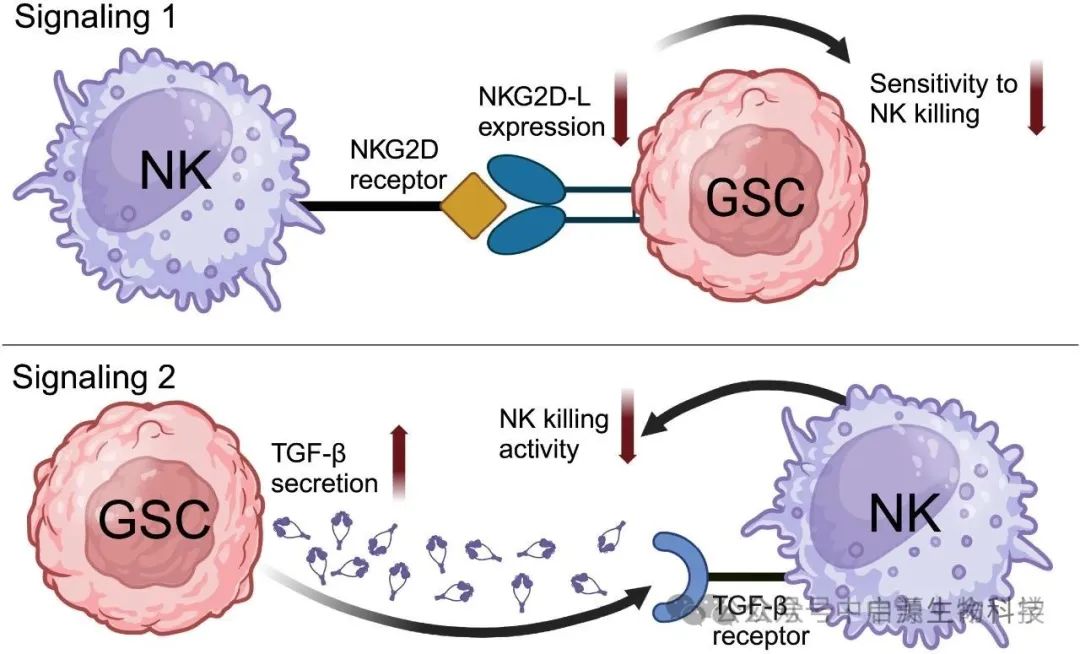
▲HGG TME中的GSC-NK相互作用
在乳腺癌转移、黑色素瘤、前列腺癌等多种肿瘤模型中,NK细胞外泌体已被证实能够显著延缓肿瘤的进展。对于神经胶质瘤,尽管相关研究仍处于早期阶段,但初步的动物实验数据已经显示出其在抑制胶质瘤干细胞增殖与侵袭方面的潜力。
此外,外泌体还可作为“药物载体”,搭载化疗药物、siRNA或靶向因子,形成“免疫+分子”的复合打击模式。简而言之,它并不是一种备选方案(“Plan B”),而是未来攻克中枢神经系统肿瘤的关键力量之一。
至此,三种策略——CAR-NK细胞、NK细胞接合器、NK细胞外泌体,已经共同构成了一个针对胶质瘤干细胞的多维免疫战术体系。
05
围剿“癌王”的意义,不只是治疗
而是重新定义免疫治疗的边界
神经胶质瘤曾被视为“绝症中的绝症”——它对放化疗具有天然的耐受性,其在脑干的位置使其隐蔽难攻,即便进行手术,也往往只能短暂延长生命。这并非一场传统意义上的“肿瘤战争”,而是一场对医学极限的持续挑战。
然而,CAR-NK细胞、NK细胞接合器和外泌体这三支源自天然杀伤细胞的免疫“特种部队”,正在以前所未有的方式,合围这位“癌中之王”的“指挥中心”——胶质瘤干细胞(GSCs)。
它们各展其能:一个突破了靶点识别的精准性,一个提升了激活效率的高效性,一个跨越了物理边界的限制性。
三条路径,汇聚成一个共同的方向:重新拓展免疫治疗的边界,踏入过去无人敢涉足的高危领域——儿童脑瘤、中枢神经系统肿瘤、超级耐药癌症。
《Molecular Therapy》这篇综述的真正意义,不仅仅在于报告疗效,更在于传递一个强烈信号:免疫治疗不仅能“治病”,更能挑战那些“被认为不可治愈的疾病”。而NK细胞,正在这场医学革命中,走向中心舞台,引领着免疫治疗的新方向。


本公众号所有文章旨在宣传生命科学领域的最新技术和研究,所有内容均不构成任何医疗指导。

本篇文章来源于微信公众号:中启源生物科技







